¿Cómo se fabrica y administra?
No empieza en un laboratorio. Empieza en el propio paciente.
Un paciente con una enfermedad grave —hasta hace poco, sin opciones reales— llega a una unidad especializada. Ahí se toma una decisión compleja, multidisciplinar, basada en criterios clínicos estrictos: avanzar hacia una terapia con terapia CAR-T.
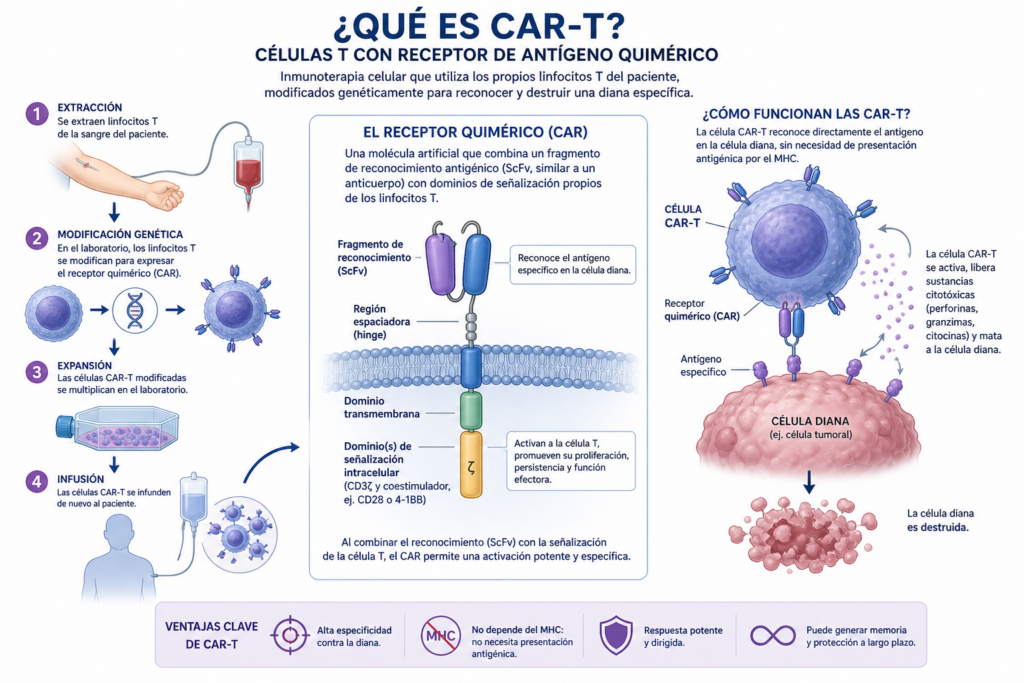
El primer paso es casi invisible, pero decisivo. Se realiza una aféresis: la sangre del paciente circula por un sistema cerrado que permite aislar selectivamente sus linfocitos T, las células ejecutoras del sistema inmunitario. El resto de los componentes sanguíneos se reinfunden en tiempo real. No es una extracción convencional; es una selección dirigida de la herramienta terapéutica que luego será rediseñada.
Esas células no vuelven inmediatamente al paciente. Se trasladan a un entorno altamente controlado, donde comienza la verdadera ingeniería biológica. En el laboratorio, bajo condiciones estrictas de Buenas Prácticas de Fabricación, los linfocitos T son modificados genéticamente para expresar un receptor quimérico: una estructura artificial diseñada para reconocer de forma precisa una diana específica. En oncología, típicamente antígenos como CD19; en enfermedades autoinmunes, el objetivo es reprogramar —o incluso reiniciar— un sistema inmunitario disfuncional.
Pero modificar no es suficiente. Es necesario amplificar. Estas células, ahora convertidas en células CAR-T, se expanden en biorreactores hasta alcanzar una masa crítica terapéutica. Hablamos de millones de células por kilogramo de peso, con variabilidad según la indicación clínica y el protocolo. Este proceso no es inmediato: requiere entre 7 y 12 días, durante los cuales cada parámetro —viabilidad celular, pureza, potencia— es monitorizado con precisión.
Cuando el producto está listo, no se administra de inmediato. Se criopreserva, deteniendo su actividad metabólica sin comprometer su funcionalidad. Días después, en el momento clínico óptimo, esas mismas células son descongeladas bajo condiciones controladas, en la propia unidad hospitalaria.
La infusión, en sí misma, es sorprendentemente sencilla: una administración intravenosa que dura entre 15 y 30 minutos. Pero reducir este proceso a ese momento sería un error conceptual. Lo que se está transfundiendo no es solo un conjunto de células; es un sistema inmunitario reprogramado con capacidad de expansión, memoria y acción dirigida.
A partir de ahí, comienza otra fase igual de crítica: el seguimiento. El paciente no solo es observado clínicamente, sino monitorizado a nivel inmunológico. Se cuantifican las células CAR-T circulantes, se evalúan subpoblaciones inmunitarias, y se analizan biomarcadores que permiten entender cómo ese nuevo sistema está interactuando con el organismo.
Nada de esto ocurre de forma aislada. Es un proceso coordinado que involucra a equipos de aféresis, inmunología, terapia celular, hematología y enfermería especializada. Cada uno cumple un rol preciso en una intervención que, en esencia, redefine el concepto clásico de tratamiento.
Porque aquí no estamos modulando el sistema inmunitario. Estamos aprendiendo, por primera vez, a reescribirlo.


 Fuentes
Fuentes